一、實驗目的
1.學習水樣的采集和預處理方法,綜合分析環境水樣中COD的含量。 2.掌握高錳酸鉀法、重鉻酸鉀法等氧化還原滴定法及分光光度法的原理及操作。
3.學習高錳酸鉀法和重鉻酸鉀法測定會水中COD的方法。 二、實驗原理
化學需氧量(COD)是指在一定條件下,用強氧化劑將水樣中的有機物等還原性物質氧化時所消耗氧化劑對應氧的質量濃度,它是評價水體受有機物污染程度的重要指標,同時也是河流和工業廢水的研究及污水處理廠的處理效果的一個重要而相對易得的參數,對它的測定是水污染分析中的常規分析工作
[1]
。
1、地表水COD的測定,根據所用氧化劑的不同,可分為高錳酸鉀法和重鉻酸鉀法,清潔的地面水、飲用水和水源水,高錳酸鉀法測定,其測定范圍為0.5~4.5mg/L,在一定程度上可以說明水體受到有機污染的狀況。該方法操作簡便、經濟、省時。
[2]
2、測定污水、工業廢水,采用重鉻酸鉀法。該類水體含有較為復雜的有機物質,往往難以氧化,宜用重鉻酸鉀法---*標法,即在酸性條件下,經重鉻酸鉀氧化處理時水樣中溶解性物質和懸浮物所消耗和重鉻酸鉀相對應的氧的質量濃度,重鉻酸鉀法對有機物的氧化較完全,適用于各種水樣,但耗時長,有危險,所耗試劑用量大。 3、用分光光度法測定廢水中的COD, 方法簡便、快速、試劑用量少( 總體積僅5 mL) , 無需移液直接用反應管當比色管, 簡化了用標準溶液標定滴定溶液的步驟, 縮短了回流時間, 近年來在工礦企業的工業廢水控制分析中廣泛使用。[3]
下面主要介紹高錳酸鉀法:
高錳酸鉀指數是指在一定條件下,以高錳酸鉀為氧化劑,處理水樣時所消耗的氧量,以氧的mg/L來表示。水中部分有機物及還原性無機物均可消耗高錳酸鉀。因此,高錳酸鉀指數常作為水體受有機物污染程度的綜合指標。
水樣加入硫酸使呈酸性后,加入一定量的高錳酸鉀溶液,并在水浴中加熱反應一定的時間:

三、主要藥品和儀器
KMnO4 固體 Na2C2O4 固體 1:3 H2SO4( 取l體積濃度為98%的濃硫酸,慢慢加入到盛有3體積水的燒杯中,攪勻。)
分析天平、電子天平、燒杯、250ml容量瓶、移液管、250ml錐形瓶、酸式滴定管、電爐、石棉網。 四、實驗步驟
1. 0.005mol/L Na2C2O4標準溶液的配制
準確稱取0.1675g經105~110oC烘干**恒重的Na2C2O4于小燒杯中加150mL蒸餾水溶解冷卻后轉移**250ml容量瓶中,定容,搖勻。 2. 0.002mol/L KMnO4溶液的配制及標定
稱取KMnO4固體約0.08g置于250ml燒杯中,加入150ml蒸餾水,使之完全溶解,溶液轉移**250ml容量瓶中,稀釋**刻度,搖勻后置于暗處放置1h,取上清液置于酸式滴定管中。
用移液管準確移取25.00ml標準Na2C2O4溶液于250ml錐形瓶中,加入5mL1:3 H2SO4在水浴上加熱到75-85oC(即開始冒蒸氣時的溫度),趁熱滴加KMnO4溶液,滴定速度由慢到快到慢的順序滴加,**溶液呈微紅色并保持30s不褪色即為終點。記錄數據,平行滴定三次。
3.水樣中耗氧量的測定
[4-5]
用移液管準確移取100.00ml水樣,置于250ml錐形瓶中加5ml 1:3 H2SO4,用滴定管準確加入10.00ml 0.002mol/L KMnO4溶液,搖勻。將錐形瓶放在電爐子上加熱**沸騰,并持續30min。取下錐形瓶,用移液管移入10.00ml Na2C2O4標準溶液、搖勻,溶液由紅色變為無色,再移入10.00ml Na2C2O4標準溶液,搖勻。趁熱用0.002mol/LKMnO4標準溶液滴定**剛出現粉紅色,并保持30s不褪色,即為終點。記錄數據。 4.空白樣耗氧量的測定
用移液管準確移取100.00ml蒸餾水,置于250ml錐形瓶中,后操作如同3操作,記錄數據。
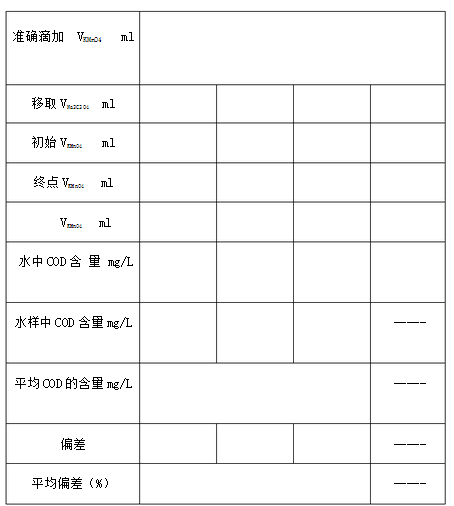
五、數據處理